#카이노스메드(284620)
-

카이노스메드 美 자회사, 파킨슨병 KM819 임상 2상 순항
[더구루=김형수 기자] 제약업체 카이노스메드의 미국 자회사 패시네이트 테라퓨틱스(FAScinate Therapeutics·이하 패시네이트)의 파킨슨병 치료제 개발에 파란불이 켜졌다. 미국에서 진행 중인 임상 2상이 순조롭게 이뤄지고 있다. [유료기사코드] 25일 업계에 따르면 패시네이트는 파킨슨 치료제 후보물질 KM-391 개발 단계는 임상 2상 파트1a에서 임상 2상 파트1b로 넘어갔다. 임상 2상 초기단계인 임상 2상 파트1a에서는 건강한 노인 피험자를 대상으로 KM-319의 약동학 및 안전성을 평가하기 위한 용량 증가 접근 방식의 실험이 이뤄졌다. 임상 2상 파트1a 결과 KM-319는 높은 용량을 투여한 경우에도 우수한 안전성을 나타냈다. 이같은 결과를 확인한 패시네이트는 임상 2상 파트1a를 종료하고 임상 2상 파트1b로 넘어갔다. 임상 2상 파트1b에서는 파킨슨 질병을 보유한 환자들을 대상으로 용량을 탐색하는 실험이 수행된다. 약동학 및 안전성을 평가하면서 KM-319 세 가지 용량으로 투여하는 방식으로 설계됐다. 고용량은 건강한 피험자를 대상으로 테스트가 이뤄진다. 패시네이트는 임상 2상 파트1b 결과를 바탕으로 임상 2상 파트2 실험에 적용할
- 김형수 기자
- 2023-03-25 06:00
-

카이노스메드, 美서 ‘KM-819’ 특허 획득…기존 약물대비 용해도 2000배 증가
[더구루=최영희 기자] 카이노스메드는 'KM-819'의 용해도를 증가시킨 염물질(salt form)의 개발 성공과 함께 이에 대한 특허를 미국에서 획득했다고 2일 밝혔다. KM-819는 카이노스메드가 파킨슨병 및 다계통위축증 치료제로 개발하여 한국과 미국에서 임상 2상 허가를 받은 후보 약물이다. 저분자 화합물로 만들어져 구강 복용제로 복용이 용이하다. KM-819는 세포의 죽음을 촉진하는 단백질인 FAF1을 저해해 신경세포의 사멸을 막고 자가포식(Autophagy) 기능의 활성화로 알파시뉴클라인이라는 단백질의 분해를 촉진하고 응집을 저해함으로써 파킨슨병의 진전을 막는 질병 조절 치료제이다. FAF1 단백질을 표적으로 개발중인 파킨슨병 치료제 후보 물질은 현재 KM-819가 유일하다. 카이노스메드는 2021년 11월 파킨슨병 치료 목적의 임상 2상에 대한 미국 FDA로 부터 IND 승인을 획득하고 4월 중 본격적인 임상을 진행할 예정이다. 다계통위축증은 국내에서 작년 10월 식약처 승인을 받고 임상 시작 준비 중이다. 아일랜드의 시장조사기관 리서치&마켓社가 공개한 보고서에 따르면 글로벌 파킨슨병 치료제 시장이 오는 2027년이면 81억 달러(한화 약
- 최영희 기자
- 2022-03-02 08:38
-

카이노스메드, 한국화학硏과 KM-819 특허권 양도 계약 체결
[더구루=최영희 기자] 카이노스메드는 최근 한국화학연구원과 뇌질환 치료제 후보물질인 KM-819의 특허권을 양도받는 계약을 체결했다고 11일 밝혔다. KM-819의 특허권은 한국화학연구원이 출원해 소유하고 있으며 카이노스메드는 2015년 한국화학연구원으로부터 기술이전을 받아, 전용실시권을 보유하고 있었다. 이번 계약을 통해 카이노스메드가 KM-819의 특허권을 보유하게 된 것이다. 카이노스메드는 지난해말 미국 FDA(식품의약국)과 국내 식품의약품안전처로부터 각각 파킨슨병 임상 2상 계획과 다계통위축증(MSA) 임상 2상 계획을 승인받았으며 본격적인 임상 개발에 돌입했다. 카이노스메드 관계자는 "특허권 양도 계약은 이미 완료한 상태이며 양도 절차를 시작했다"며 "카이노스메드는 특허권 소유자로서 앞으로 기술이전에 유리한 입장에 있게 됐다"고 말했다. 카이노스메드는 이외에도 KM-819의 용도특허 등 다른 2종의 특허를 출원해 놓은 상태다.
- 최영희 기자
- 2022-01-11 10:57
-

카이노스메드 에이즈치료제, 中건강보험 목록 ‘등재'...판매 본격화
[더구루=최영희 기자] 이노스메드가 개발해 중국으로 기술수출한 에이즈 치료제가 중국 건강의료보험 목록에 등재됐다. 향후 중국 시장에서 판매가 본격화될 전망이다. 카이노스메드는 6일 중국 파트너사인 장수아이디(Jiangsu Aidea Pharmaceuticals)의 에이즈 치료제 아이노베린(Ainuovirine, 상품명 Aibond®)이 중국 '국민기초의료보험, 산업재해보험 및 출산보험 약품목록'에 등재됐다고 밝혔다. 아이노베린은 카이노스메드가 한국화학연구원으로부터 초기에 도입한 에이즈 치료 물질(KM-023)로 국내에서 임상 1상까지 완료했으며 2014년 장수아이디로 기술이전했다. 장수아이디는 이 물질을 도입한 이후 ACC007이라는 물질명으로 개발하고 있으며 테노포비르(TDF), 라미부딘(3TC)과 함께 처방하는 방식으로 지난해 임상 3상을 성공적으로 마치고, 최근 중국 최초의 경구용 에이즈 치료제로 신약판매 최종허가(NDA)를 받았다. 장수아이디는 아이노베린이 건강의료보험에 등재됨에 따라 1조원이 넘는 중국 시장에서 판매가 크게 늘어날 것으로 기대하고 있다. 장수아이디측은 "아이노베린이 시판 승인을 받은 이후 6개월도 지나지 않아 건강의료보험목록에 등재된
- 최영희 기자
- 2021-12-06 08:11
-

카이노스메드, 파킨슨병 치료제 미국 FDA 임상2상 IND 승인
[더구루=최영희 기자] 카이노스메드는 16일 자회사인 패시네이트 테라퓨틱스(FAScinate Therapeutics, 미국 샌디에고)를 통해 제출한 KM-819의 파킨슨병에 대한 임상 2상 임상시험계획서(IND)를 미국 식품의약국(FDA)이 승인했다고 밝혔다. 적응증을 확대한 다계통위축증(MSA) 치료제의 임상 2상 IND를 국내 식품의약품안전처로부터 지난달 승인 받은데 이은 것으로 KM-819의 임상 개발이 국내외에서 본격화되게 됐다. 카이노스메드는 임상 사이트들과의 계약 이후 환자 모집에 나서게 되며, 임상 2상을 크게 두 부분으로 나눠 진행할 계획이다. 건강하고 나이 많은 참가자 18명과 파킨슨병 환자 24명을 각각 대상으로 KM-819를 200㎎, 400㎎, 800㎎씩 투여해 적정 용량을 확정할 예정이다. 임상1상에서는 부작용 없이 400 mg까지 투여했다. 용량이 결정되면 미국내 병원에서 환자 288명을 대상으로 2년간 임상을 진행하게 된다. 그동안 카이노스메드가 진행해 온 특정 유전자(GBA) 변이가 있는 환자의 줄기세포를 이용한 실험에서 효능을 확인함에 따라 이번 임상에 유전자 변이 환자를 포함하기로 했다. KM-819는 세포의 죽음을 촉진하는
- 최영희 기자
- 2021-11-16 10:16
-
1

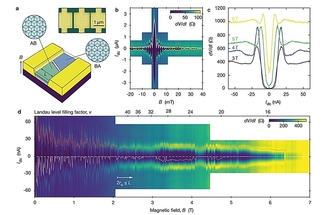
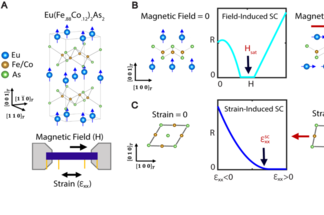
노벨상 수상자 참여한 연구팀, '1차원 시스템 활용' 초전도체 연구결과 발표
22770 -
2

[단독] LG엔솔·포스코 '세계 1위 매장국' 칠레 리튬 개발 사업 출사표
19853 -
3

中 기반 드론 제조업체 DJI, 미국서 퇴출 직면
19627 -
4

삼성중공업, 델핀 FLNG 4기 추가 수주 기대감↑
17748 -
5

[단독] HD현대 찾아온 수에즈운하청장…'그린 카날' 사업 협력 제안
15313 -
6

사우디, 리튬 수입한다…전기차 배터리 생태계 구축 전력
14928 -
7

[단독] 삼성전자, 美 GPU 엔지니어 채용 나서...엑시노스 부활 신호탄
14157
-
중국
중국서 불법 유통, 엔비디아 H100 GPU 가격 하락 국면
[더구루=정예린 기자] 중국에서 비밀리에 불법 거래되는 엔비디아의 인공지능(AI) 칩 가격이 신제품 출시 소식에 힘입어 소폭 하락세에 접어들었다. 미국의 대중(對中) 제재 강화 조치에도 불구하고 엔비디아 칩 수요가 급증하며 밀수 시장 규모가 커지고 있다. 2일 대만연합신문망(UDN)에 따르면 최근 중국 밀수 시장에서 엔비디아의 첨단 그래픽저장장치(GPU) 'H100' 가격이 떨어지고 있다. 올 2분기 엔비디아 GPU 신제품 'H200' 출시를 앞두고 현지 판매 업자들이 재고 정리에 나서면서다. 300만 위안(약 5억7000만원)을 호가했던 중국 내 H100 거래가는 현재 약 270만~280만 위안(약 5억1000만~5억3000만원) 수준에 형성돼 있다. 하락하기 전 가격은 공식 판매가인 28만~30만 달러(약 3억9000~4억1000만원)보다 약 50% 높은 수준이다. 미 상무국 산업안보국(BIS)이 지난달 공식 시행한 대중국 수출 규제 개정안에 따라 H100과 H200은 중국 수출이 공식적으로 금지돼 있다. 하지만 불법 유통 채널을 통한 거래는 활발하게 진행되고 있다. 높은 수요에 대비해 비축해뒀던 재고가 시장에 풀리며 가격 조정 이뤄진 것이다. 판매자들은

-
미국
스텔란티스, 수소 트럭 램 HD 5500 EV 미국 시장 출시 '예고'
[더구루=윤진웅 기자] 세계 4위 완성차 업체 스텔란티스(Stellantis)가 미국 시장에 수소 구동 트럭을 선보인다. 새로운 수소 연료 전지 기술을 탑재해 주행 성능을 높이는 등 상품성을 갖추게 될 것으로 기대된다. [유료기사코드] 2일 업계에 따르면 스텔란티스는 픽업트럭 전문 브랜드 램을 통해 미국 시장에 수소 구동 트럭 HD 5500 EV를 선보이겠다는 계획이다. 이는 장 미셸 빌리그(Jean-Michel Billig) 스텔란티스 수소 모빌리티 최고기술책임자(CTO)가 직접 밝힌 내용이다. 구체적인 출시 시기를 언급하지는 않았지만, 해당 트럭을 현재 램 HD 픽업 트럭 생산을 맡고 있는 멕시코 공장에서 생산할 것이라고 스텔란티스 측은 예고했다. 구체적인 성능과 제원은 출시 시기에 맞춰 공개할 예정이다. 현재까지 정보를 종합하면 HD 5500 EV에는 스텔란티스 2세대 수소 연료 전지 기술 탑재가 유력하다. 해당 전지는 수소 트럭을 위해 개발된 기술인 만큼 최장 약 500km 주행이 가능한 것으로 알려졌다. 이번 수소트럭 개발에 있어 토요타와의 협업은 따로 없는 것으로 전해진다. 실제 스텔란티스는 지난 2022년 토요타와 수소차 협력 가능성을 원천 차단