[더구루=오소영 기자] 삼성바이오에피스의 유방암 바이오시밀러(복제약) SB3가 세계보건기구(WHO)의 사전적격성평가(PQ)를 통과했다. 저개발 국가에 보급돼 높은 치료 비용으로 혜택을 보지 못했던 유방암 환자들의 생존율을 높이는 데 기여할 전망이다.
19일 업계에 따르면 삼성바이오에피스 네덜란드 법인은 최근 WHO로부터 SB3에 대한 사전적격성평가(PQ) 인증을 받았다. 트라스투주맙 성분을 활용한 복제약으로 WHO의 사전적격성평가 인증을 받은 것은 SB3가 최초다.
이는 SB3가 품질과 효능, 안전성 측면에서 WHO의 기준을 충족했다는 의미다. 유엔 기구들이 해당 백신을 WHO의 권고에 따라 질병 위험 국가에 공급할 수 있다.
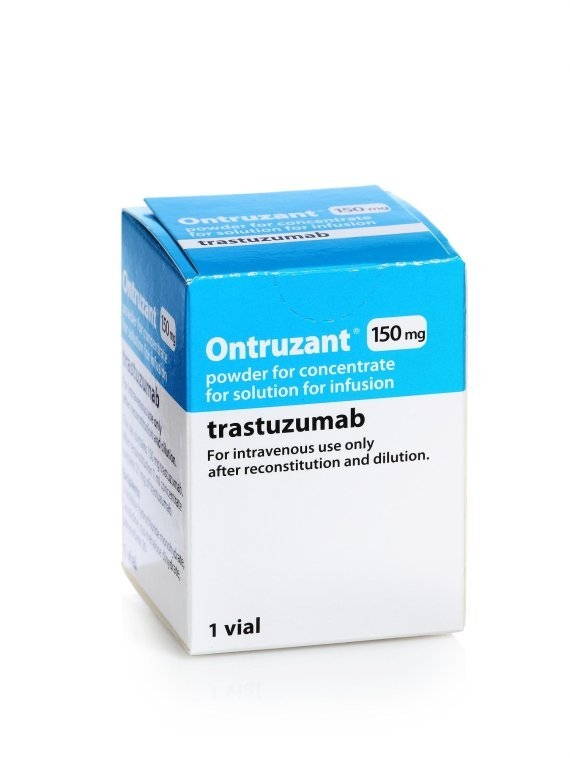
SB3는 다국적제약사 로슈가 제조·판매하는 오리지널 '허셉틴'의 바이오시밀러다. 허셉틴보다 저렴하면서 효능은 비슷하다. 삼성바이오에피스 조사 결과 SB3를 맞은 환자의 1년간 무사건 생존율은 96.7%으로 허셉틴(94.3%)과 차이가 적었다. 전체 생존율은 SB3 100%, 허셉틴 99.4%였다.
SB3는 유럽(온트루잔트), 한국(삼페넷) 등에 출시됐다. 올 1월에는 미국 식품의약국(FDA)으로부터 SB3의 미국 최종 판매 허가를 획득한 바 있다.
이번에 WHO의 인증을 받으며 유방암 치료 비용을 획기적으로 낮추고 완치율을 높일 것으로 기대된다. 유방암은 전 세계 여성이 가장 많이 걸리는 질병 중 하나다. WHO는 유방암 환자 수가 2040년 310만명에 이를 것으로 진단했다.
특히 저·중소득 국가에서 가장 많이 증가할 것으로 전망되는 가운데 이들 국가의 환자들은 고비용으로 치료를 받기 어려운 실정이다. WHO의 자체 설문조사(1325명 대상) 결과 사하라 이남 아프리카 지역 3개국에서 412명(약 31%)이 1년 이내에 암 치료를 받지 못하는 것으로 나타났다.
테드로스 아드하놈 게브레예수스 WHO 사무총장은 "모든 여성들은 효과적이고 저렴한 유방암 치료를 받을 수 있는 권리를 갖고 있다"며 "SB3의 PQ 인증은 전 세계 여성들에게 희소식이 될 것"이라고 밝혔다.